临床医学检验中影响血液细胞检测质量的有关因素及其控制方法探讨
作者:admin 来源:未知 日期:2021-04-09 08:52人气:
摘 要:
目的 探究临床医学检验中影响血液细胞检测质量的有关因素及控制方法。方法 选取2018年1月至2019年12月本院收治的150例血型相同且符合血液细胞检测条件的受检者作为研究对象,通过设置不同受检条件,分析影响血液细胞检测质量的因素。结果 稀释比例1∶10 000的各项血液细胞检测结果均高于1∶5 000,差异有统计学意义(P<0.05)。室温环境下不同放置时间各项血液检测结果比较差异有统计学意义(P<0.05)。低温环境下不同放置时间各项血液检测结果比较差异有统计学意义(P<0.05)。同一放置时间下,室温与低温环境下的各项血液检测结果差异有统计学意义(P<0.05)。结论 血液细胞检测过程中,血液稀释比例、血液样本放置时间和放置温度均会对检测结果产生影响,在未来临床医学检测工作中要严格把控血液细胞检测的各个环节,尽量避免不良因素对检测结果造成影响,确保检测结果的准确性。
关键词:
临床医学检测 血液细胞 检测质量 影响因素 控制方法
Discussion on the factors influencing the quality of blood cell test and the control methods in clinical medicine test
LU Yang
Department of Clinical Laboratory, Taian City Maternal and Child Health Hospital;
Abstract:
Objective To explore the relevant factors and control methods that affect the quality of blood cell testing in clinical medical testing.Methods A total of 150 patients with the same blood type and qualified blood cell test conditions from January 2018 to December 2019 in our hospital were selected as study subjects. By setting different test conditions, the factors affecting the quality of blood cell test were analyzed. Results Each blood cell test result with a dilution ratio of 1:10 000 was higher than that of 1:5 000, and the difference was significant(P<0.05). There was significant difference in blood test results under different storage time at room temperature(P<0.05). The difference of blood test results was statistically significant in different storage time under low temperature environment(P<0.05). At the same storage time, there was significant difference in blood test results between room temperature and low temperature environment(P<0.05). Conclusion In the process of blood cell detection, blood dilution ratio, blood sample storage time and temperature will affect the test results. In the future clinical medical test work, we must strictly control all aspects of blood cell testing, try to avoid adverse factors affecting the test results, and ensure the authenticity of the test results.
Keyword:
Clinical medicine test; Blood cell; Test quality; Influencing factors; Control methods;
血液细胞检测又被称为血常规检测,是当前临床检测中的重要部分[1]。其检测项目主要包括白细胞(white blood cell,WBC)、红细胞(red blood cell,RBC)、血红蛋白(hemoglobin,HGB)、血小板(platelets,PLT)等[2]。其检测结果不仅可以反映血液相关指标的变化,为诊断、治疗提供依据;还可以辅助医生更加准确的判断疾病,选择更加有效的治疗方案[3]。但临床实践发现,在医学检测过程中因受多种因素的影响,血液细胞检测结果可能会存在一定的误差,从而影响病情的判断[4]。对影响血液细胞检测结果的有关因素进行分析并提出有针对性的控制方法,是提高血液细胞检测质量的关键[5]。本研究选取2018年1月至2019年12月本院收治的150例血型相同且符合血液细胞检测的受检者作为研究对象,旨在探究临床医学检测中影响血液细胞检测质量的有关因素及控制方法,现报道如下。
1 资料与方法
1.1 临床资料
选取2018年1月至2019年12月本院收治的150例血型相同且符合血液细胞检测的受检者进行研究,其中男77例,女73例;年龄27~56岁,平均年龄(41.5±7.2)岁。
1.2 纳入及排除标准
纳入标准:身体各项指征均符合本研究要求;意识清醒,智力、认知水平正常;配合度较高,能遵从研究要求,积极配合各项研究工作;本研究经医院伦理委员会批准,患者均自愿参与研究并签署知情同意书。排除标准:存在肿瘤等恶性疾病或其他严重器质性疾病者;临床资料不完整,或因为各种原因不能完成研究者。
1.3 方法
抗凝剂稀释比例:在患者空腹状态下,利用静脉采血法采集受检者的下肘静脉血液样本。分别用1∶10 000和1∶5 000稀释比例的抗凝剂进行处理,然后将相同稀释比例的血液标本进行混合,摇匀后将其分为75等份送检[6]。血液样本放置情况:利用上述方式再次采集受检者的血液样本,将其混合摇匀后等分为300份。其中150份在室温条件下储存,分别在放置30、60及180 min时各选取50份样本进行检测[7]。剩余的150份样本在22℃的低温环境下储存,同样在30、60及180 min时各选取50份样本进行检测[8]。检测所用仪器及药物:一次性静脉真空采血管[碧迪医疗器械(上海)有限公司],EDTA-K2抗凝剂(北京凯瑞基生物科技有限公司),T540型血细胞自动分析仪(英国库尔特公司)。
1.4 观察指标
通过对比法统计分析150例受检患者血液样本在不同稀释比例、不同放置时间和不同放置温度下的检测结果,检测指标包括WBC、RBC、PLT和HGB。
1.5 统计学方法
采用SPSS 20.0统计学软件进行数据处理,计量资料以“”表示,行t/F检验,多组间进行F检测,以P<0.05为差异有统计学意义。
2 结果
2.1 稀释比例对血液细胞检测结果的影响
稀释比例1∶10 000的各项血液细胞检测结果均高于稀释比例1∶5 000的,且组间差异均有统计学意义(P<0.05)。其中稀释比例1∶5 000的RBC:(4.1±0.3)×1012/L,稀释比例1∶10 000的RBC:(5.8±0.7)×1012/L,组间差异有统计学意义(t=19.331 5,P=0.000 0)。稀释比例1∶5 000的WBC:(6.4±0.8)×109/L,稀释比例1∶10 000的WBC:(9.6±1.2)×109/L,组间差异有统计学意义(t=19.215 3,P=0.000 0)。稀释比例1∶5 000的HGB:(106.5±12.8)g/L,稀释比例1∶10 000的HGB:(166.3±15.3)g/L,组间差异有统计学意义(t=25.961 4,P=0.000 0)。稀释比例1∶5 000的PLT:(136.4±21.3)×1012/L,稀释比例1∶10 000的PLT:(189.6±26.1)×1012/L,组间差异有统计学意义(t=13.676 1,P=0.000 0),见图1。
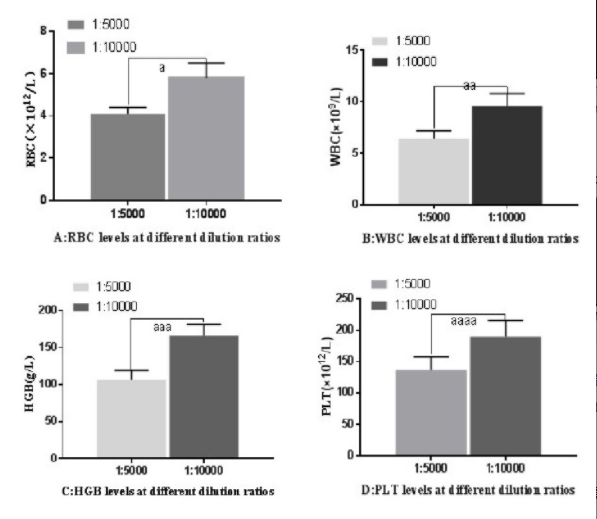

2.2 血液放置情况对血液细胞检测结果的影响
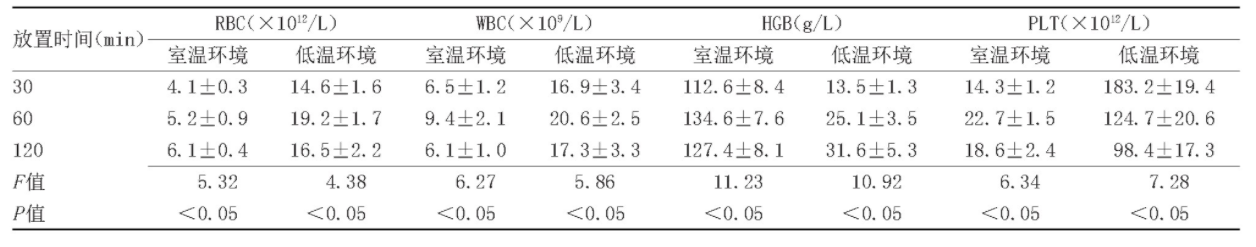
室温环境下不同放置时间各项血液检测结果比较差异有统计学意义(P<0.05);低温环境下不同放置时间各项血液检测结果比较差异有统计学意义(P<0.05);同一放置时间下,室温与低温环境下各项血液检测结果比较差异有统计学意义(P<0.05);不同放置时间下室温与低温环境中血液细胞RBC水平差异有统计学意义(30 min:t=45.609 0,P=0.000 0;60 min:t=51.465 0,P=0.000 0;120 min:t=32.887 6,P=0.000 0)。不同放置时间下室温与低温环境中血液细胞WBC水平比较差异有统计学意义(30 min:t=20.396 0,P=0.000 0;60 min:t=24.256 2,P=0.000 0;120 min:t=22.967 4,P=0.000 0)。不同放置时间下室温与低温环境中血液细胞HGB水平差异有统计学意义(30 min:t=82.440 3,P=0.000 0;60 min:t=92.537 7,P=0.000 0;120 min:t=69.981 0,P=0.000 0)。不同放置时间下室温与低温环境中血液细胞PLT水平差异有统计学意义(30 min:t=61.444 5,P=0.000 0;60 min:t=34.919 6,P=0.000 0;120 min:t=32.307 4,P=0.000 0),见表2。
表2 血液放置情况对血液细胞检测结果的影响
3 讨论
3.1 影响血液细胞检测质量的因素
血液检测结果可以直观反映患者的各项机体生化指标,是医师判断患者疾病种类的重要依据[9]。如果其检测结果的误差较大则会影响患者的治疗方式,导致预后效果不佳[10]。所以控制血液细胞检测质量对临床疾病的判断及治疗具有重要意义[11]。但在实际的临床医学检验工作中,血液细胞检测质量受多方面因素的影响,从而导致血液检测结果出现偏差[12]。
本研究发现,在血液细胞检测过程中,血液稀释比例,血液放置时间以及血液放置温度均会对各项血液检测结果产生影响,且以上影响因素组间差异均具有统计学意义(P<0.05)。这与王富伟[7]的研究结果相似,即血液稀释比例1∶5 000和1∶10 000的各项血液检测结果(WBC、RBC、PLT和HGB)差异均有统计学意义(P<0.05),且室温下血液样本放置时间不同,各项血液检测结果存在差异。
3.2 血液细胞检测质量的控制方法
本研究仅从稀释比例、血液放置时间及血液放置温度3个方面进行对比分析,而在临床实践中影响血液检测质量的因素较复杂。所以在血液检测中,参与检测的医务人员要按照医学检验的规范流程进行操作,仔细排查可能造成影响的因素,同时进行记录总结,进一步优化临床医学检查的工作路径,最大程度上控制监测质量。对血液细胞检测质量的控制可以从检测前、检测时、检测后3个方面入手,具体方法如下。
3.2.1 检测前
(1)对参与检测的医务人员进行相关技能教育培训,确保其具备高水平的专业技能及综合素质。(2)严格按照医院的规定血液细胞检测流程操作,熟练掌握检测中的各项注意事项。(3)熟知检测相关仪器及设备在检测过程中可能存在的问题,并掌握解决措施。(4)减少标本采集中的不良因素,检测前对血液细胞的相关信息进行控制。
3.2.2 检测时
(1)对检测所用的试剂和药品进行检查,确定其是否在规定的标准范围之内。(2)检查血液检测中所用到的仪器及设备是否可以正常使用。(3)对检测湿度及湿度进行控制,确保其在规定的标准检测范围之内。(4)检测时参与检测的医务人员在做好本职工作的基础上相互监督配合,最大程度降低不良因素。
3.2.3 检测后
(1)检测结束并不意味着检测工作的完成,此时需要对获得检测数据进行统计分析。(2)在数据分析的基础上,要综合患者的临床资料,过往疾病史和整体身体状态,确定患者的细胞直方图和病理特征。(3)如果有条件的情况下,还可以借助显微镜对患者的血液细胞进行进一步检查,从而更加做出更加准确的病理判断,为治疗方案的制定提供更为有效的数据。
综上所述,在血液细胞检测过程中,血液稀释比例和样本放置时间、放置温度均会对其检测结果产生影响,在未来临床医学检测工作中要严格把控血液细胞检测的各个环节,尽量避免不良因素对检测结果造成的影响,确保检测结果的准确性。
参考文献
[1]张争鸣,杜晓娟.临床医学检测中影响血液细胞检测质量的有关因素及其控制方法探讨[J].中国实用医药,2018,13(19):76-77.
[2]Adams Charleen D,Boutwell Brian B.A Mendelian randomization study of telomere length and blood-cell traits[J].Sci Rep,2020,10:12223.
[3]涂建华,赵红梅.临床医学检测中影响血液细胞检测质量的有关因素及其控制方法[J].名医,2018(3):80.
[4]Zheng Xin Ting,Tan Yen Nee.Development of Blood-CellSelective Fluorescent Biodots for Lysis-Free Leukocyte Imaging and Differential Counting in Whole Blood[J].Small,2020,16:e1903328.
[5]孟丽.探讨临床医学检测中影响血液细胞检测质量的相关因素及其控制方法[J].中国医药指南,2018,16(23):160-161.
[6]Wang Jia-Qiang,Zhang Juan,Wang Zhi-Bin,et al.Analysis of Ig G Subclass in Blood Serum between Multiple Myeloma and Lymphoma Patients and Its Correlation with Blood Cell Parameters[J].Zhongguo Shi Yan Xue Ye Xue Za Zhi,2020,28:1957-1961.
[7]王富伟.临床医学检测中血液细胞检测的质量控制方法探究[J].临床研究,2019,27(8):22-23.
[8]Amalia Lisda,Dalimonthe Nadjwa Zamalek.Clinical significance of Platelet-to-White Blood Cell Ratio (PWR)and National Institute of Health Stroke Scale (NIHSS) in acute ischemic stroke[J].Heliyon,2020,6:e05033.
[9]赵于菱.临床医学检测中影响血液细胞检测质量的相关因素及其控制方法[J].医药前沿,2017,7(35):216-217.
[10]Chen LF,Zhuang JM,Zhang JR,et al.[Study on the effect of direct anti-human globulin test positive strength on patients'red blood cell transfusion][J].Zhonghua Yi Xue Za Zhi,2020,100:3510-3514.
[11]臧义英.临床医学中血液细胞检测质量控制的相关影响因素[J].当代医学,2016,22(27):36-37.
[12]Ko K,Klamer G,Trickett A,et al.Enumeration of primitive haematopoietic progenitor cells to improve the quality of cord blood product testing[J].Cytotherapy,2019,21(5):S54.


